Il primo Talk Show del percorso FAD ECM “Approccio sistematico all’encefalopatia epatica: oltre la variabilità clinica”, tenutosi il 26 maggio scorso e realizzato con il contributo non condizionato di Alfasigma, ha dato avvio a un percorso di formazione articolato in tre appuntamenti, che complessivamente forniranno 36 crediti ECM.
Il corso, attivo in modalità asincrona fino al 31 dicembre 2025, è stato progettato con l’obiettivo di promuovere una discussione articolata sulla gestione strutturata e condivisa della EE, superando le attuali disomogeneità cliniche e organizzative.
Il talk show ha previsto un’interazione continua con i partecipanti, grazie alla possibilità di porre domande in tempo reale tramite chat, alle quali i relatori hanno risposto nel corso della discussione finale. I quesiti emersi hanno evidenziato l’interesse per la gestione ambulatoriale delle forme lievi, l’uso dei lattulosio-based agents e la valutazione neurocognitiva standardizzata.
Attraverso i rispettivi contributi tematici i Proff. Paolo Caraceni, Vincenza Calvaruso e Lorenzo Ridola hanno delineato le basi per un approccio sistematico all’EE, sottolineando l’importanza di criteri diagnostici condivisi e di strumenti efficaci per la stratificazione del rischio.
Il paziente con EE: fragile, complesso, multidimensionale
Tra i primi temi affrontati dalla faculty vi è stata l’identificazione del paziente tipo, ovvero il soggetto affetto da cirrosi epatica che sviluppa l’encefalopatia epatica, una complicanza neuropsichiatrica potenzialmente grave. Il Prof. Lorenzo Ridola ha introdotto la discussione inquadrando l’EE come manifestazione tipica dei pazienti con cirrosi avanzata (classificata come encefalopatia tipo C), sottolineandone l’elevata eterogeneità clinica, con quadri che vanno dalle forme minime e subcliniche fino al coma epatico.
Come ha sottolineato il prof. Caraceni, questi pazienti raramente presentano una sola complicanza: la EE si inserisce in un contesto di cirrosi scompensata, con ascite, varici esofagee, ittero, malnutrizione e sarcopenia. L’EE peggiora la qualità di vita, riduce l’autonomia e aumenta il carico assistenziale, rendendo indispensabile una presa in carico precoce e integrata.
La Prof.ssa Calvaruso ha ricordato che spesso il paziente non è consapevole dei sintomi iniziali dell’EE, soprattutto nelle forme minime.
Il riconoscimento precoce è dunque affidato al medico di medicina generale e al contesto familiare, che possono cogliere variazioni comportamentali lievi ma significative: rallentamento mentale, modifiche dell’umore, dimenticanze, difficoltà a svolgere compiti abituali. Dal punto di vista epidemiologico, il paziente tipo è maschio, di età medio-avanzata, con cirrosi nota (spesso virale o alcol-correlata), ma si osserva oggi un incremento dei casi anche tra le donne, complice l’evoluzione dei fattori eziologici.
Il messaggio chiave che emerge è che il paziente con EE è spesso un paziente fragile, complesso, multidimensionale, per il quale la diagnosi precoce e l’approccio integrato rappresentano requisiti indispensabili per preservare la qualità della vita e ottimizzare l’efficacia delle cure.
Meccanismi patogenetici: il ruolo centrale dell’ammoniaca
Il Prof. Ridola ha illustrato i principali meccanismi fisiopatologici alla base di questa condizione, che colpisce circa un terzo dei pazienti cirrotici nel corso della loro storia clinica. L’EE è definita come una disfunzione cerebrale secondaria a insufficienza epatica e/o shunt portosistemici, con manifestazioni cliniche che spaziano dalle forme minime fino al coma.
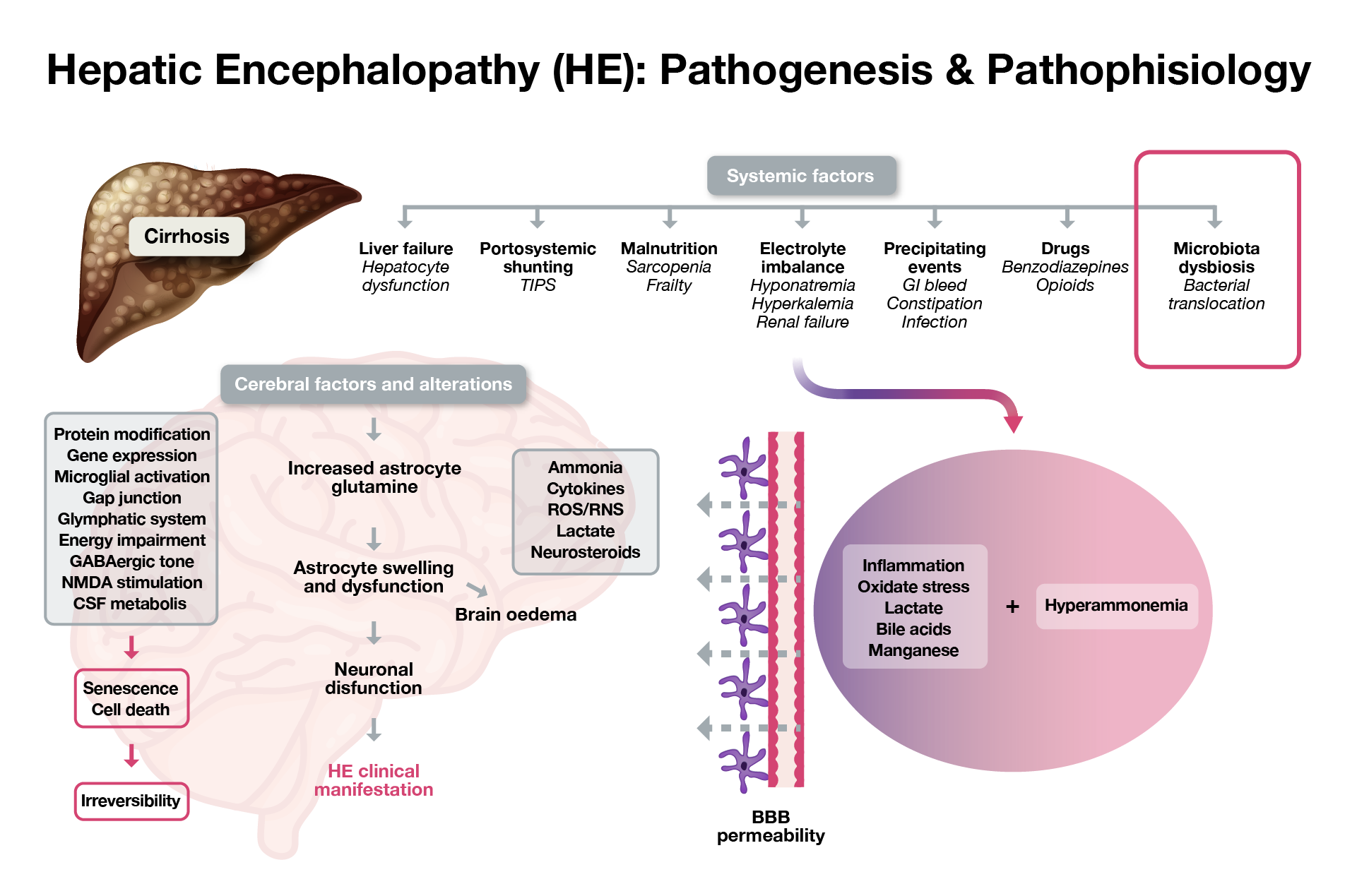
Elemento centrale della patogenesi è l’accumulo sistemico di ammoniaca, proveniente principalmente dall’intestino.
In condizioni fisiologiche, l’ammoniaca viene neutralizzata dal fegato e in parte da muscoli e reni. Nei pazienti con cirrosi scompensata o shunt portosistemici, l’ammoniaca bypassa il fegato, supera la barriera ematoencefalica e provoca neurotossicità a livello centrale.
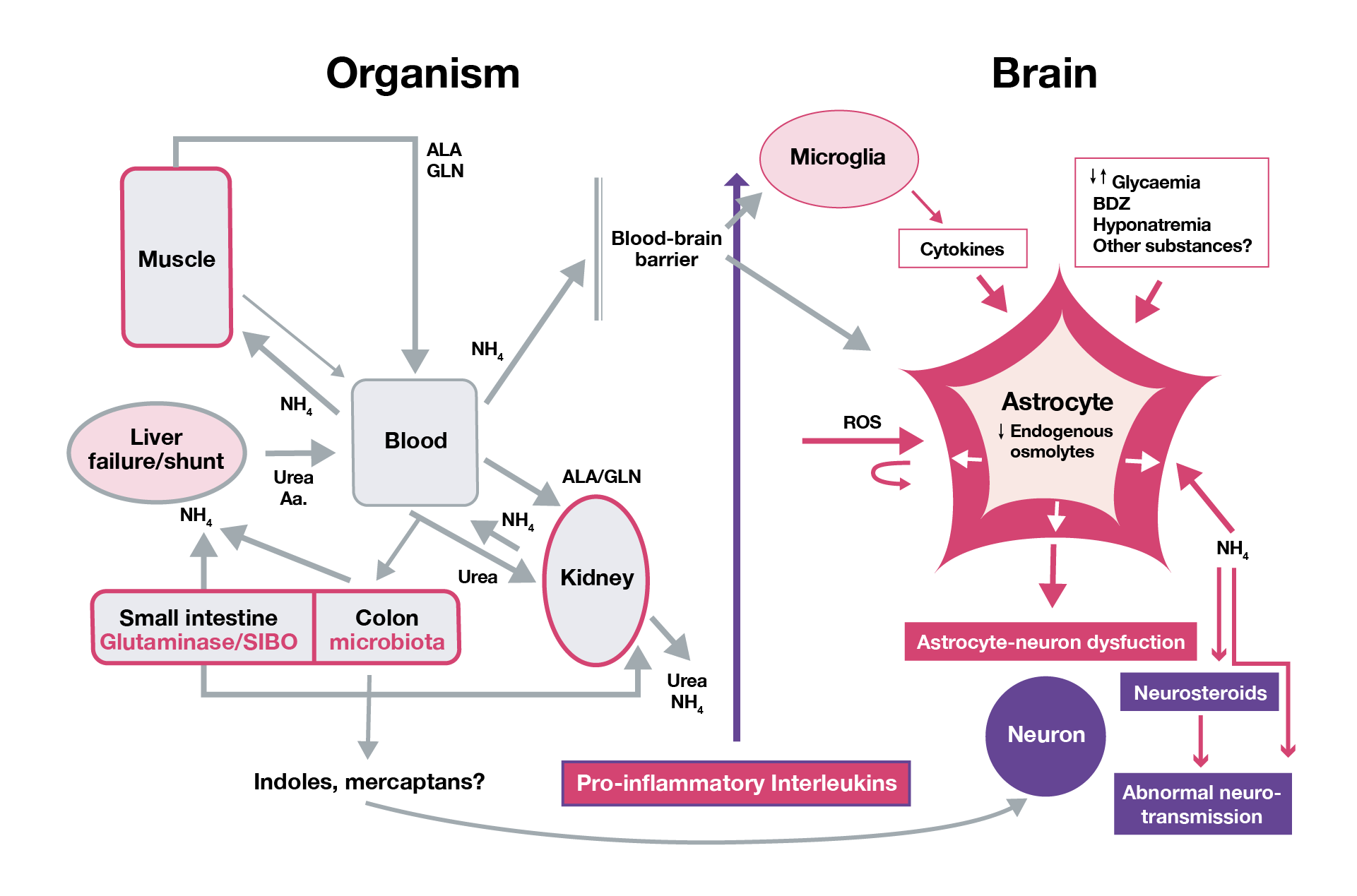
A questa si sommano altri fattori: disbiosi intestinale, traslocazione batterica, infiammazione sistemica e produzione di citochine proinfiammatorie, che concorrono a creare un ambiente tossico per il sistema nervoso centrale.
Nonostante la misurazione dell’ammoniemia non sia sempre correlata alla gravità clinica, rimane un parametro utile da integrare con l’osservazione clinica, specie nei casi sospetti.
Il Prof. Ridola ha quindi fatto riferimento alle più recenti linee guida dell’European Association for the Study of the Liver (EASL), che sottolineano come, in presenza di un sospetto clinico di encefalopatia epatica, la misurazione dell’ammoniemia plasmatica sia raccomandata come supporto diagnostico. Tuttavia, è stato evidenziato che tale parametro non può sostituire la valutazione clinica, né è sempre correlato alla gravità del quadro neurologico: va pertanto interpretato con cautela e inserito in un contesto valutativo più ampio.
Sarcopenia ed encefalopatia: un circolo vizioso
Un tema centrale del primo incontro è stato il legame tra EE e sarcopenia, una condizione di progressiva perdita di massa e funzione muscolare che si associa frequentemente alla cirrosi epatica, in particolare nei pazienti con encefalopatia.
Il termine, coniato nel 1988, deriva dal greco (“sarx” = carne, “penia” = perdita) e nel tempo è stato oggetto di definizioni operative più precise.
Attualmente, la definizione proposta dall’European Working Group on Sarcopenia in Older People prevede tre criteri: sospetto clinico in presenza di riduzione della forza muscolare, conferma tramite evidenza di perdita di massa muscolare, e classificazione come severa in presenza di compromissione funzionale. La prevalenza della sarcopenia è alta anche nei pazienti non ancora scompensati (30%) e raggiunge il 70-80% nei casi più avanzati.
Il Prof. Caraceni ha spiegato che la perdita di massa e funzione muscolare riduce la capacità detossificante del muscolo sull’ammoniaca (tramite la glutammina sintetasi), aggravando l’ipertossiemia. Al tempo stesso, l’encefalopatia favorisce inattività fisica, la malnutrizione e un ulteriore declino muscolare, generando un circolo vizioso che peggiora la prognosi e la qualità di vita.
La sarcopenia può essere valutata con diversi strumenti. Il gold standard per la diagnosi nei pazienti con cirrosi resta la tomografia computerizzata (TAC), con misurazione della sezione trasversale del muscolo scheletrico a livello della vertebra L3. Questo esame permette non solo di quantificare la massa muscolare, ma anche di valutarne la qualità, ad esempio identificando la presenza di infiltrazione grassa (miosteatosi), spesso associata a un peggior esito clinico.
Strategie terapeutiche: nutrizione, esercizio, integrazione e aderenza
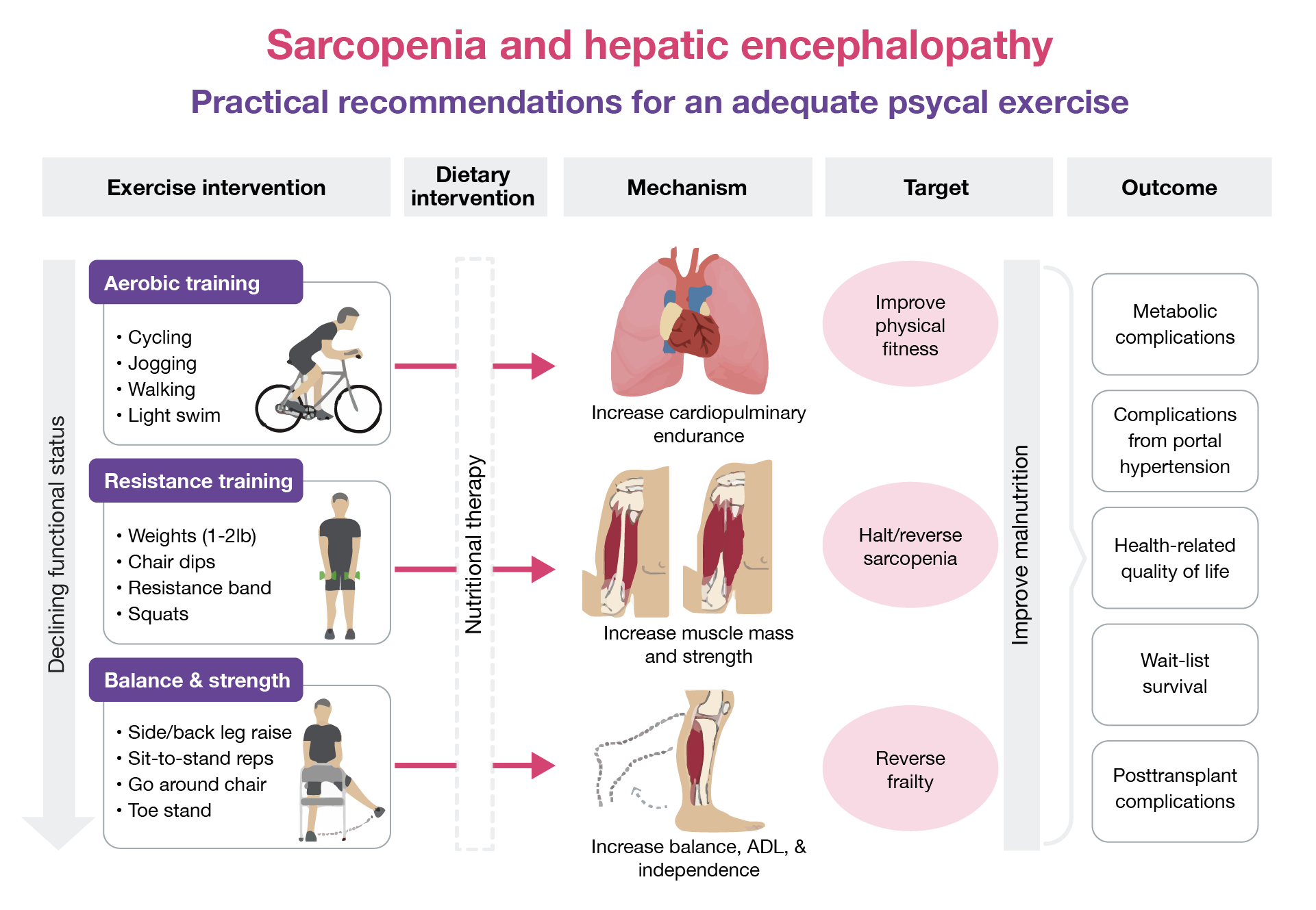
Il trattamento della sarcopenia nel paziente cirrotico si fonda su:
- Attività fisica adattata alle capacità del paziente, includendo esercizi sia aerobici che di resistenza muscolare (esercizi con pesi leggeri);
- Intervento nutrizionale strutturato, con le seguenti indicazioni:
35–40 kcal/kg/die;
1,2–1,5 g di proteine/kg/die, preferendo fonti vegetali e lattiero-casearie;
suddivisione in 5–6 pasti al giorno e spuntino serale (60–70 g di carboidrati prima di dormire) per prevenire il catabolismo notturno;
evitare diete iposodiche severe, che riducono la palatabilità e l’introito calorico;
integrazione, se carenti, di zinco, vitamina D, vitamina B1;
possibile utilizzo di integratori come la leucina o suoi derivati (β-Hydroxy β-Methylbutyrate).
È stato anche menzionato l’interesse verso l’impiego di androgeni anabolizzanti, sebbene riservato a casi selezionati e ancora oggetto di ricerca. Il Prof. Caraceni ha sottolineato la necessità di un approccio multidisciplinare che coinvolga epatologi, nutrizionisti, fisioterapisti, infermieri e caregiver, anche perché l’aderenza al piano terapeutico resta una delle maggiori criticità nei pazienti con cirrosi avanzata.
Ospedalizzazione, infezioni e sostenibilità della gestione clinica
Un altro aspetto discusso riguarda l’elevato impatto dell’ospedalizzazione, sia in termini clinici che economici. I costi per la gestione di un paziente con EE possono superare i 14.000 euro l’anno. Le infezioni, spesso contratte in ambiente ospedaliero, sono oggi considerate una complicanza quasi “strutturale” della cirrosi. Possono innescare l’insorgenza di ACLF (acute-on-chronic liver failure), con coinvolgimento multiorgano e alta mortalità. Anche infezioni apparentemente minori, come quelle urinarie, possono accelerare il declino clinico.
È dunque fondamentale rafforzare i percorsi di gestione territoriale, ridurre i ricoveri non necessari e garantire una presa in carico precoce ed efficace. In quest’ottica, il test degli animali (animal naming test) rappresenta uno strumento semplice ed efficace per il riconoscimento precoce dei disturbi cognitivi, già validato a livello internazionale e facilmente utilizzabile anche dai MMG.
Un nuovo profilo epidemiologico e la sfida della prevenzione
Il Prof. Caraceni ha infine illustrato l’evoluzione del profilo epidemiologico della cirrosi. Le forme virali, un tempo predominanti, sono oggi in netto calo grazie agli antivirali, mentre aumentano le forme metabolico-alcoliche. Il binge drinking, l’obesità infantile e la sindrome metabolica rappresentano fattori di rischio in crescita. L’Italia è oggi tra i Paesi europei con la più alta prevalenza di sovrappeso e obesità in età scolare. Diventa quindi urgente promuovere la prevenzione primaria, l’educazione alimentare e l’attività fisica fin dalla giovane età, anche attraverso il coinvolgimento delle scuole e delle istituzioni. La sostenibilità futura del SSN dipenderà anche dalla capacità di ridurre l’incidenza delle malattie epatiche croniche legate allo stile di vita.
Prossimi appuntamenti e iniziative
Al termine dell’incontro, sono stati forniti take-home messages sintetici, volti a rafforzare i concetti chiave emersi nel corso della discussione e a orientare la pratica clinica quotidiana. Il secondo modulo del corso approfondirà la diagnosi differenziale nei pazienti con alterazioni neurologiche, le traiettorie cliniche della cirrosi avanzata e l’impiego di scale e strumenti classificativi per l’assessment multidimensionale. Interverranno anche i Proff. Giacomo Germani e Stefano Fagiuoli, con focus sul TIPS e sul trapianto di fegato.
È stato inoltre annunciato il Clinical Talent Contest, riservato a giovani medici specialisti. Gli Autori dei tre migliori casi clinici, selezionati dal Comitato Scientifico, saranno invitati a partecipare ad un live webinar in cui presenteranno il proprio lavoro, e avranno la possibilità di pubblicarlo su Clinical Practice e HEpatic-Lab.com, e parteciperanno gratuitamente al Congresso AISF 2026.

Lascia un commento